"Esta es una acción de rutina que tiene que darse siempre que haya una enfermedad potencialmente inexplicable en uno de los ensayos", aseguró la portavoz de la farmacéutica, Michelle Meixel, en un comunicado.
"En pruebas a gran escala habrá enfermedades por casualidad, pero deben revisarse de forma independiente para verificar esto con cuidado", insistió la vocera.
Y hasta las autoridades de salud de México -uno de los países llamados a participar en la fabricación de la vacuna- pidieron no sacar las cosas de proporción como producto del anuncio.
"Quiero dejar claro, no hay que anticipar vísperas, no empezar a especular sobre la seguridad, en general de las vacunas, y en particular de esta que está involucrada porque no tenemos la información correspondiente", dijo el subsecretario de salud mexicano Hugo López Gatell.
Y, efectivamente, todavía es demasiado pronto para saber si los problemas de salud que motivaron la hospitalización del voluntario que participaba en la fase tres de los ensayos clínicos en Reino Unido fueron provocados por la vacuna.
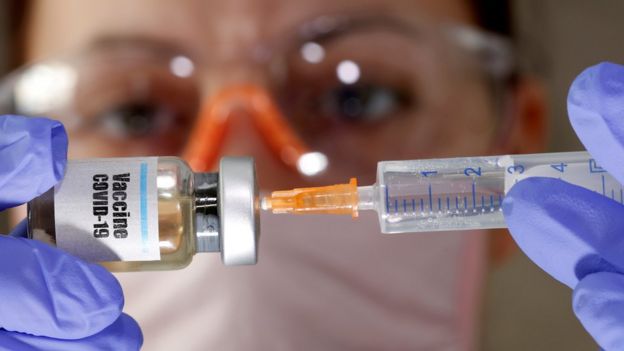 Derechos de autor de la imagenREUTERS
Derechos de autor de la imagenREUTERSSegún The New York Times, el voluntario fue diagnosticado con mielitis transversa, un síndrome inflamatorio que afecta la médula espinal y puede ser causada por infecciones virales, pero también por otros trastornos de la mielina, como la esclerosis múltiple.
Esto todavía no ha sido confirmado por AstraZeneca, que insistió en que "la situación está siendo investigada por un comité independiente y es demasiado pronto para concluir el diagnóstico específico".
Y el carácter "rutinario" de este tipo de medidas también fue destacado por el corresponsal en temas de salud de la BBC, Fergus Walsh, quien informó que esta es de hecho la segunda pausa en los ensayos de Oxford y AstraZeneca "desde que los primeros voluntarios fueron inmunizados en abril".
¿Buena noticia?
A primera vista, puede parecer alarmante: un ensayo de una vacuna -y no cualquier vacuna, sino una que recibe una grandísima atención mundial- se pospone debido a una sospecha de reacción adversa grave", reconoció Walsh.
"Pero tales eventos no son inauditos", destacó el periodista de la BBC.
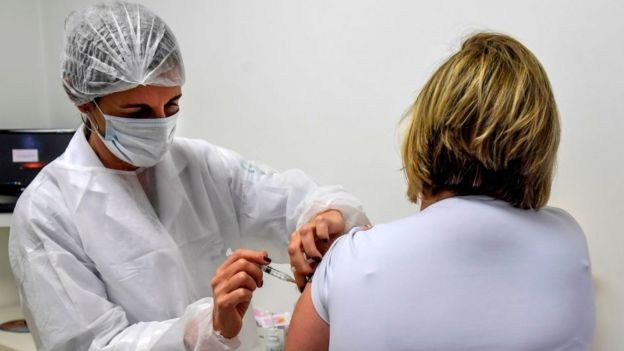 Derechos de autor de la imagenAFP
Derechos de autor de la imagenAFP"Cuando se tienen más de 18.000 adultos en pruebas en todo el mundo, en algún momento alguien se va a enfermar. Y si hay alguna duda (acerca de las causas) lo correcto es hacer una pausa e investigar", explicó Walsh.
Y en lo mismo insistió Sir Jeremy Farrar, un experto en control de enfermedades infecciosas y director del Wellcome Trust, una organización benéfica de investigación biomédica con sede en Londres.
"Yo he sido tanto un investigador como un participante en este tipo de pruebas de vacunas, y a menudo hay pausa. Pero para mí esto solo subraya lo importante que es que este tipo de ensayos se hagan correctamente, que haya supervisión independiente y que podamos confiar en los reguladores", le dijo a la BBC.
"Sí, las pausas son comunes, pero tenemos que tomarlas en serio. Cada una de estas pausas debe ser tomada en serio", insistió.
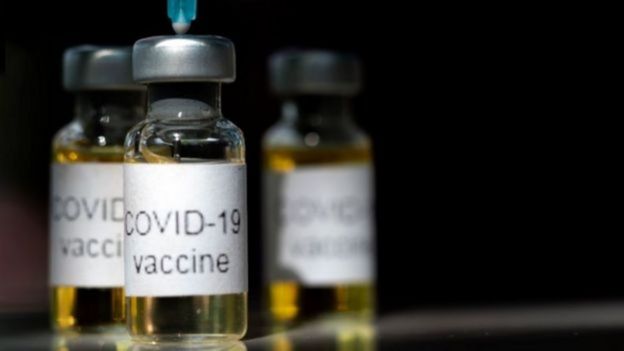 Derechos de autor de la imagenGETTY IMAGES
Derechos de autor de la imagenGETTY IMAGESCarmen Álvarez Domínguez, profesora de Procesos Sanitarios en la Facultad de Educación e investigadora en Inmunoterapia de la Universidad Internacional de La Rioja, considera que la suspensión temporal de las pruebas puede considerarse "una buena noticia" por varias razones.
En un articulo en The Conversation la experta señala que la pausa "refleja que las agencias de regulación están pendientes de los ensayos clínicos en vacunas no solo en la fase final al liberar los resultados, sino en los análisis rutinarios".
Además, considera que esto muestra que "las compañías farmacéuticas son las primeras en priorizar la seguridad y transparencia en sus vacunas, y paralizar los ensayos hasta que un Comité Externo evalúe clínica y científicamente dicho efecto adverso".
Para Álvarez, "cuanto más se detallen efectos adversos de una vacuna en preparación, mejor se podrá mejorar su formulación y decidir a que grupos de la población se debe excluir, fundamental para la vacunación a gran escala".
Por lo pronto, la suspensión temporal de las pruebas se produce justo un día después de nueve grandes farmacéuticas, incluida Astrazeneca, se comprometieran públicamente a mantener los más altos estándares éticos y científicos en la búsqueda de una vacuna contra el coronavirus.
Según Fergus Walsh, el equipo de la Universidad de Oxford cree que la pausa "demuestra que están comprometidos con la seguridad de sus voluntarios y con los más altos estándares de conducta en sus estudios".
El futuro
Astrazeneca, sin embargo, también dijo que estaba trabajando para "acelerar" la revisión del caso, "para minimizar cualquier impacto potencial en el cronograma del ensayo".
Según el corresponsal de temas de salud de la BBC, una decisión sobre la continuación de las pruebas podría tomarse en materia de días.
 Derechos de autor de la imagenGETTY IMAGES
Derechos de autor de la imagenGETTY IMAGES"Hasta entonces todos los lugares de vacunación en Reino Unido, Brasil, Sudáfrica y Estados Unidos estarán paralizados", destacó Walsh.
López Gatell, sin embargo, fue más cuidadoso con respecto a los posibles tiempos de reanudación de las pruebas.
"Hay situaciones que se resuelven en 24 horas o 72 horas y ya se reactivan, pero si es algo que requiere otro tipo de investigaciones más detalladas en los tejidos humanos, en los líquidos humanos, en la historia clínica de la persona afectada, se requerirá más tiempo", explicó el funcionario mexicano.
"Es difícil predecir cuánto durará la suspensión", agregó, luego de explicar que como México no está participando en las pruebas clínicas, la única suspensión de las mismas para el país sería "que se retrase el momento de llegada de vacuna".
A menos, claro está, que el peor escenario se confirme y las pruebas no logren confirmar la seguridad del producto.
La vacuna que desarrollan la Universidad de Oxford y AstraZeneca utiliza una versión genéticamente modificada del adenovirus que causa el resfriado común en los chimpancés.
Y según sus competidores rusos, "a diferencia de los muy bien estudiados vectores adenovirales humanos (como el que ellos emplean para su vacuna Sputnik V), no hay estudios de largo plazo para vacunas innovadoras basadas en ARNm y adenovirus de monos".

- MAPA: Alcance global del coronavirus
- PREGUNTAS CLAVE: Cuáles son los síntomas y cómo se transmite
- TRATAMIENTOS: Cómo están combatiendo el coronavirus
- PREVENCIÓN: Qué puedes hacer para evitar el contagio

Recuerda que puedes recibir notificaciones de BBC Mundo. Descarga la nueva versión de nuestra app y actívalas para no perderte nuestro mejor contenido.